मिल गई कैंसर की संजीवनी? 6 महीने में ही पूरी तरह ठीक हो गए मरीज, दवा का ‘चमत्कार’
वॉशिंगटन
चिकित्सा क्षेत्र में विकास के बावजूद कैंसर जैसी बीमारी को आज भी असाध्य रोग की श्रेणी में रखा जाता है। हालांकि अब एक क्लीनिकल ट्रायल के बाद दावा किया जा रहा है कि जिन मरीजों पर प्रयोग किया गया उनको 100 प्रतिशत सार्थक परिणाम मिले हैं और वे पूरी तरह कैंसर से मुक्त हो गए। अगर भविष्य में भी यह दवा कारगर रहती है तो इसे कैंसर के लिए संजीवनी ही कहा जाएगा।
मरीजों के साथ हुआ चमत्कार
क्लीनिकल ट्रायल के तौर पर रेक्टल कैंस के 18 मरीजों पर यह प्रयोग किया गया था। इन मरीजों को 6 महीने तक डोस्टरलिमैब नाम की दवा दी गई। दावा किया गया है कि अब ये सभी मरीज पूरी तरह कैंसर से मुक्त हैं। न्यूयॉर्क टाइम्स की रिपोर्ट के मुताबिक डोस्टरलिमैब नाम की दवा लैब में विकसित अणुओं से बनी है जो कि मानव शरीर में सब्स्टीट्यूट एँटीबॉडीज के तौर पर काम करती है।
गायब हो गए ट्यूमर
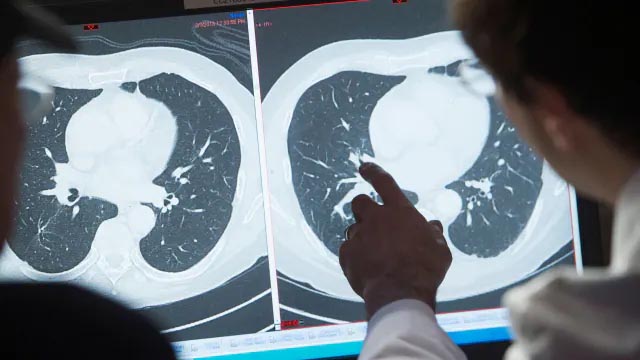
जिन मरीजों को यह दवा दी गई थी उनके ट्यूमर धीरे-धीरे गायब हो गए। इन सभी मरीजों में कैंसर का नामोनिशान नहीं रह गया। इनका फिजिकल एग्जाम, एंडोस्कोपी, पॉजिट्रोन एमिशन टोमोग्राफी और पीईटी स्कैन के साथ ईएमआई भी कराया गया। न्यूयॉर्क के मेमोरियल स्लोन कैटरिंग सेंटर के डॉ. लुइस ए डियाज के मुताबिक इतने दिनों के इतिहास में यह पहली बार संभव हो पाया है कि एक तरह के इलाज से ही सभी मरीज पूरी तरह ठीक हो गए।
हैरान हैं चिकित्सा क्षेत्र के लोग
न्यूयॉर्क टाइम्स के मुताबिक कैंसर का इलाज करवाने के दौरान किसी भी मरीज को कीमोथेरपी, सर्जली और रेडिएशन जैसे दर्दनाक प्रॉसेस से गुजरना पड़ता है। इस वजह से कई अन्य बीमारियां भी हो जाती हैं। लेकिन इस क्लीनिकल ट्रायल से जो नतीजे मिले हैं उनसे वैज्ञानिक भी हैरान हैं। जिन मरीजों को लगा था कि उनका इलाज का यह एक चरण भर है। अब उन्हें पूरी तरह से बीमारी से मुक्ति मिल चुकी है। यानी अब आगे उन्हें इलाज की जरूरत ही नहीं है। मीडिया से बात करते हुए डॉ. एलन पी वेनूक ने कहा कि यह बहुत ही आश्चर्य की बात है कि सभी मरीजों में कैंसर का नामोनिशान खत्म हो गया। यह दुनिया की पहली ऐसी रिसर्च है। ट्रायल के तौर पर डोस्टरलिमैड को हर तीसरे हफ्ते 6 महीने तक दिया गया। खास बात यह है कि इस दवा के कोई साइड इफेक्ट नहीं दिखायी दिए हैं।





